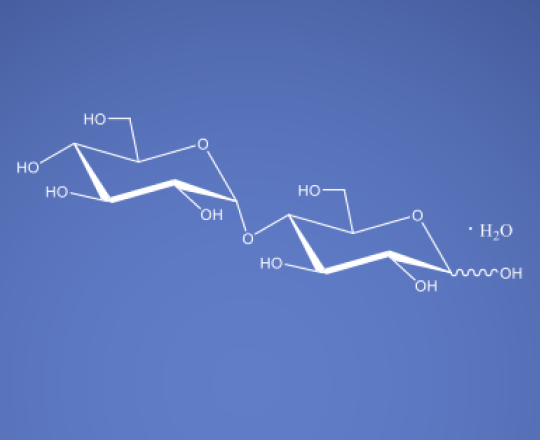
Pfanstiehl Maltose Monohydrate Citation Page
Menú
Menú
- Hogar
- Soluciones
- Estabilización de vacunas y productos biológicos
- Reducción de la agregación de proteínas
- Reducción de la viscosidad
- Formulaciones de alta concentración
- Mitigación de la degradación del polisorbato
- Formulaciones biológicas por inhalación
- Formulaciones de anticuerpos biespecíficos y triespecíficos
- Soluciones químicas complejas
- Excipientes con bajo contenido de metales
- Excipientes bajos en nitrosamina
- Productos
-
- Servicios
- Publicaciones
- Sobre nosotros
- Noticia
- Contáctenos